Диабетическая болезнь почек – одно из наиболее значимых осложнений сахарного диабета (СД). Медианный возраст диагностики данной патологии при СД 1 типа (СД1) – 25 лет [1], при СД 2 типа (СД2) – 59,71 года [2]. Ежегодный прирост числа пациентов с СД2 составляет в среднем 7,1% во всех возрастных группах [3]. При этом наблюдается омоложение популяции пациентов с СД2 [4], что в свою очередь имеет негативный прогноз в отношении распространенности в популяции микро- и макрососудистых осложнений и увеличения бремени заболеваний сердечно-сосудистой системы и почек, включая хроническую болезнь почек (ХБП) [5]. Анализ данных регистра пациентов с СД в РФ за период 2010–2022 гг. обнаружил, что среди всех осложнений СД рост отмечен лишь для двух позиций: ХБП на 13,69% и хронической сердечной недостаточности на 2,67 [6]. Патология почек при СД в большей степени характерна для пациентов с заболеваниями периферических артерий (ЗПА): по имеющимся данным у пациентов с СД2, ЗПА и диабетической нефропатией (ДН) отмечалась в 38,1% случаев по сравнению с 11,9% в группе СД2 без ЗПА [7]. Снижение физической и социальной активности вследствие осложнений СД, прежде всего вследствие ХБП, приводит к значимому снижению качества жизни (КЖ) пациентов [8, 9]. Анализ динамики показателей КЖ как часть оценки эффективности инструментов фармакотерапии, направленных на лечение ДН и ХБП у пациентов с СД, является одним из актуальных направлений исследований, позволяющих получить наиболее полные данные о лекарственном препарате и перспективах его дальнейшего применения.
Инструменты оценки КЖ при СД и ХБП
Общими (универсальными) опросниками, которые среди всех прочих заболеваний могут быть использованы у пациентов с СД и ХБП, являются SF-36, SF-12 и EQ-5D. SF-36 включает 36 пунктов в 8 доменах (категориальные ответы, оцениваются по шкале от 0 до 100, где 100 означает лучшее состояние здоровья), оценивает физический и психический компоненты (PCS и MCS соответственно) [10]. SF-12 – сокращенная проверенная версия SF-36 [11].
EQ-5D – один из наиболее применяемых опросников КЖ, разработан в 1990 г. [12]. Первая часть состоит из 5 параметров, измеряющих мобильность, самообслуживание, обычную активность, боль и депрессию. Вторая часть имеет 20-сантиметровую визуальную аналоговую шкалу с конечными точками, помеченными как «наилучшее вообразимое состояние здоровья» и «наихудшее вообразимое состояние здоровья», привязанными к 100 и 0 соответственно. EQ-5D и ряд его модификаций наиболее часто применяются для оценки КЖ, в т.ч. у пациентов с СД, т.к. требует минимум времени выполнения и нагрузки для пациентов и медицинских работников [13–15].
Диабет-специфичные опросники КЖ созданы для более чувствительной оценки влияния на различные сферы жизни пациента инсулинотерапии, необходимости в постоянном мониторинге сахара крови, эпизодов гипогликемии, использования устройств для непрерывного мониторинга глюкозы крови и инсулиновых помп, для оценки влияния на КЖ осложнений, характерных именно для СД. Среди множества диабет-специфических инструментов оценки КЖ наиболее используемые включают ADDQoL и версии DQoL. Все они могут применяться у пациентов с СД и диабетической болезнью почек, тем не менее существуют также опросники КЖ, специфичные для оценки влияния диабетической болезни почек на КЖ пациентов с СД: DDRQOL, а также его сокращенные версии DDRQOL-R и DDRQOL-R-9.
В табл. 1 приведены основные характеристики наиболее часто используемых опросников КЖ, разработанных специально для пациентов с СД.
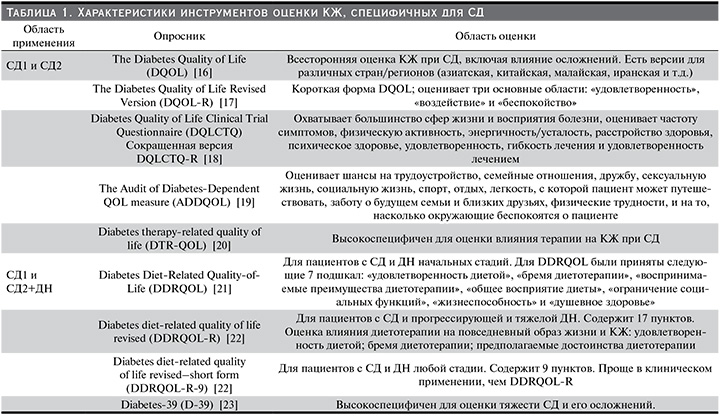
КЖ у пациентов с СД и ХБП
Согласно результатам мета-анализа 98 исследований (n=9400), направленных на оценку КЖ пациентов с различными заболеваниями при помощи опросника EQ5D, уровень КЖ пациентов с СД достаточно высок со средним значением 0,83 (95% доверительный интервал [ДИ]: 0,77–0,90). Однако при этом важно отметить, что самые высокие показатели КЖ были отмечены среди пациентов с СД без ДН (0,99), а наименьшие значения были отмечены среди пациентов с коморбидными состояниями на гемодиализе (0,31). При этом, если рассматривать отдельно ХБП, то среднее значение КЖ значительно ниже и составило 0,7 (95% ДИ: 0,48–0,92) [24].
По данным сравнительного исследования КЖ в Польше, было установлено, что средний индекс по опроснику EQ-5D-5L составил 0,797±0,251 для пациентов с СД против 0,932±0,130 для пациентов без СД [25]. Сравнительная оценка КЖ с использованием EQ-5D в популяции пожилых пациентов с СД и без СД выявила, что для первой группы в большей степени характерны проблемы с мобильностью (отношение шансов [ОШ]= 1,57, 95% ДИ: 1,33–1,85), самообслуживанием (ОШ=1,65, 95% ДИ: 1,35–2,01), ежедневной деятельностью (ОШ= 1,78, 95% ДИ: 1,51–2,11), болью/дискомфортом (OШ=1,42, 95% ДИ: 1,24–1,64) и тревожностью/депрессий (OШ= 1,33, 95% ДИ: 1,07–1,64) [26]. По данным работы, оценивавшей КЖ пациентов с СД2 в Индии с использованием опросника WHO QoL-BREF, было обнаружено, что среднее итоговое значение составило 58,03+18,293, что соответствует низкому КЖ. Среднее значение физического компонента КЖ составило 58,64+18,541, психологического – 62,21+21,313, социального – 45,25+22,698, компонента окружающей среды – 66,03+15,390; среднее итоговое значение составило 58,03+18,293 [27].
Осложнения СД значительно снижают КЖ: при использовании опросника EQ-5D-5L у пациентов с осложнениями СД2 значение составило 0,55+0,29 против 0,70±0,28 у пациентов без осложнений (р<0,001) [28]. Аналогичные тенденции были обнаружены и в исследовании КЖ пациентов с СД2 в Кувейте, где более низкое КЖ было связано с осложнениями СД, коморбидностью, а также принадлежностью к женскому полу, ожирением (индекс массы тела – ИМТ≥30), инсулинотерапией и низким уровнем образования [29]. Многопараметрическая регрессионная модель Тобита при оценке КЖ у пациентов с СД2 в Эфиопии выявила следующие достоверные предикторы низкого КЖ [15]: осложнения СД, инсулинотерапию, ожирение, длительный период после установления диагноза СД, пожилой возраст, гипергликемию натощак и коморбидность. Значимое снижение КЖ у пациентов с СД2 на фоне осложнений и сопутствующих заболеваний было продемонстрировано и в работе E.L.Y. Wong и соавт. (2020). После поправки на социально-экономические и демографические факторы использованная авторами модель показала, что респонденты с СД2 и двумя дополнительными хроническими заболеваниями с большей вероятностью будут демонстрировать более низкий показатель индекса КЖ (EQ-5D-5L) [30]. Наличие трех сопутствующих заболеваний было определено предиктором более низкого КЖ при диабете в работе M. Jeong (2020) [31].
ХБП является одним из лидирующих осложнений СД, прогрессирование которого влияет на КЖ. Национальное исследование в Южной Корее продемонстрировало снижение КЖ (EQ-5D) у пациентов с СД на фоне прогрессирования ХБП. Оценка КЖ осуществлялась в популяции пациентов с СД (n=7243), из которых ХБП любой стадии отмечалась у 24% (n=1768), ХБП 3–5-й стадий – у 8,6% (n=775). Средний индекс EQ-5D составил для пациентов с СД без патологии почек 0,92±0,002, для СД и ХБП 1–2-й стадий – 0,93±0,004, для СД и ХБП 3-й стадии – 0,86±0,0, для СД и ХБП 4–5-й стадий – 0,79±0,02 [8].Анализ КЖ пациентов с СД и ХБП с использованием опросника KDQoL™-36 (Kidney Disease and Quality of Life) обнаружил, что каждая последующая стадия ХБП является фактором риска приблизительно двукратного ухудшения композитных показателей физического и ментального компонентов, симптоматики ХБП, эффекта ХБП и бремени ХБП [32]. В свою очередь наличие СД у пациентов с ХБП также является фактором риска снижения КЖ, что подтверждают результаты проспективного многонационального исследования, включившего пациентов с ХБП (Австралия, Новая Зеландия, Канада и Испания, n=1696, опросник EuroQoL 5) [33]. По результатам оценки КЖ (опросники KDQOL™-36, SF-12) пациентов с ХБП – участников исследования C-STRIDE (n=2742) было установлено, что пациенты с СД и ХБП характеризовались минимальным значением КЖ по сравнению с пациентами лишь с ХБП. Они также были старше и имели более низкий уровень образования, бóльшую длительность фармакотерапии и более высокую распространенность сердечно-сосудистых заболеваний, чем пациенты с ХБП без СД (р<0,05) [34].
Влияние терапии на КЖ пациентов с СД и ХБП
Лонгитюдное исследование длительностью 12 месяцев оценивало влияние на КЖ (опросник KDQOL) нового комплексного метода ведения пациентов с СД и ХБП. Результаты обнаружили отсутствие значимой отрицательной динамики показателей КЖ, также было отмечено, что показатель симптоматики ХБП и композитный физический компонент значительно улучшились у женщин, лишь немного ухудшившись у мужчин [35]. Продемонстрированные результаты указывают на первостепенное значение правильного терапевтического подхода к предотвращению ухудшения КЖ пациентов с СД и ХБП. Повышение КЖ пациентов с СД2 прежде всего ориентировано на предотвращение развития новых осложнений и замедление прогрессирования уже имеющихся, прежде всего нефропатии и ХБП. Если ХБП уже присутствует, основной задачей является борьба с дальнейшим усугублением состояния почечной функции. Международные клинические рекомендации по ведению пациентов с СД и ХБП включают три основные группы препаратов: ингибиторы ренин-ангиотензин-альдостероновой системы (иРААС – ингибиторы ангиотензин-превращающего фермента [иАПФ] и блокаторы рецепторов ангиотензина II – БРА), ингибиторы натрий-глюкозного котранспортера 2-го типа (иНГЛТ-2) и нестероидный селективный антагонист минералокортикоидных рецепторов (нсАМКР) – финеренон.
Основная информация о роли и месте указанных групп препаратов в ведении пациентов с СД2 и ХБП, согласно последним данным международных клинических рекомендаций (ADA – American Diabetes Association, 2023) [36] и KDIGO – Kidney Disease: Improving Global Outcomes, 2022 [37]) представлена в табл. 2.
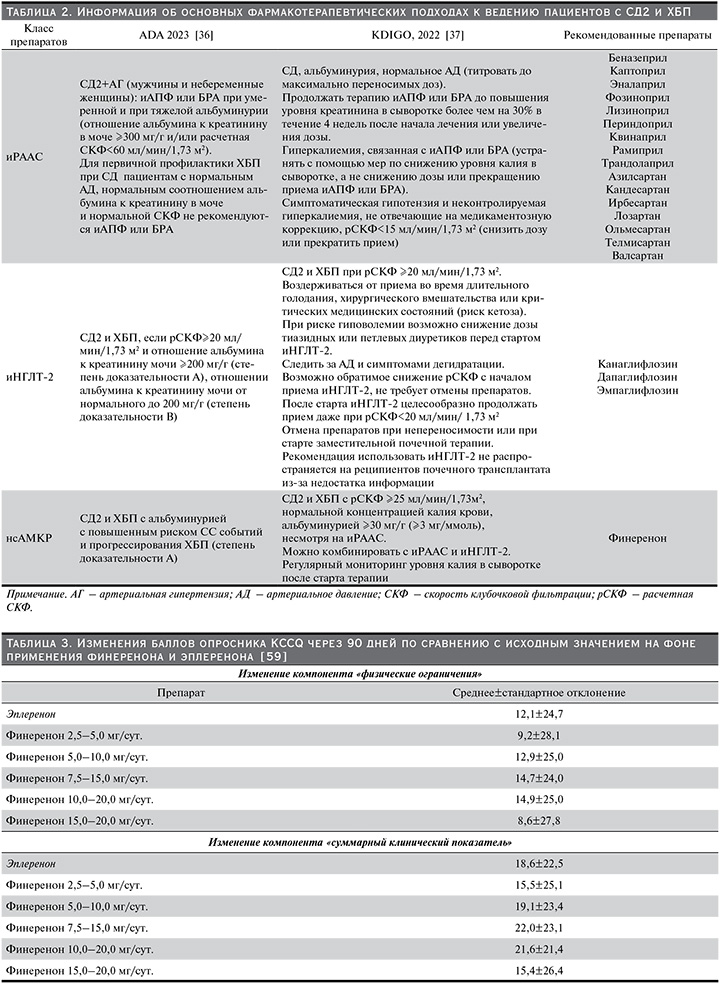
Алгоритмы специализированной медицинской помощи больным сахарным диабетом, опубликованные в 2023 г. и ориентированные на ведение пациентов с СД и со всеми сопутствующими патологиями, в т.ч. и с ХБП, на территории Российской Федерации в целом аналогичны международным рекомендациям и также включают 3 группы препаратов: иРААС, иНГЛТ-2 и финеренон [38].
Эффективность указанных в рекомендациях трех групп препаратов для терапии ХБП у пациентов с СД, равно как и эффективность основных групп сахароснижающих препаратов доказаны в многочисленных исследованиях. В частности, мета-анализ 816 исследований (n=471 038), оценивавших 13 различных классов препаратов, обнаружил, что у пациентов с СД наиболее эффективными с точки зрения предотвращения терминальной стадии ХБП, смерти от всех причин и госпитализаций по поводу сердечной недостаточности являлись иНГЛТ2, аналоги и агонисты глюкагоноподобного пептида-1 и финеренон. Также финеренон характеризовался как препарат с минимальным риском гипогликемии среди всех средств [39]. Клиническая эффективность должна находить свое отражение в положительной динамике показателей КЖ пациентов. Рассматривая исследования, выполненные с целью анализа КЖ в зависимости от типа получаемой терапии, можно остановиться на следующих.
В работе K.P.J. Smits и соавт. (2018) оценивалось КЖ 1044 пациентов с СД2 в Нидерландах. Целью исследования была проверка гипотезы о влиянии назначений фармакотерапии в соответствии с рекомендациями и собственно бремени фармакотерапии, специфичной для диабета, на КЖ пациентов (опросники EQ5D-3L и WHO-5). Средний балл по опроснику EQ-5D-3L составил 0,86 (IQR=0,81–1,00). Анализ чувствительности с использованием идеальных баллов по шкале EQ5D-3L против всех прочих значений опросника указал на старт иАПФ как на наиболее предпочтительный вариант терапии. ОШ достижения идеального балла по шкале EQ5D-3L составило для иАПФ 3,09 (95% ДИ: 1,11–8,59) [40]. Важным итогом исследования было отсутствие негативного влияния на КЖ применения комбинаций лекарственных средств, включая сахароснижающие препараты и иРААС, что подтверждает гипотезу о превалировании эффектов клинической эффективности во влиянии на КЖ по сравнению с неудобством, связанным с необходимостью применять несколько лекарственных средств.
Положительное влияние иАПФ на КЖ пациентов с СД2 на фоне различной выраженности микро- и макроальбуминурии было продемонстрировано в анализе «затраты–полезность». Авторы показали максимально положительное влияние как на КЖ, так и на стоимость болезни тактики применения у всех пациентов с СД2 иАПФ (или БРА при непереносимости иАПФ) как можно в более ранние сроки с целью предотвращения терминальной стадии почечной недостаточности и летального исхода вследствие ХБП [41]. Аналогичный анализ, осуществленный в Китае (2018), также подтвердил полезность назначения иАПФ/БРА всем пациентам с СД2 в отношении снижения рисков прогрессирования ХБП с точки зрения как КЖ, так и снижения затрат [42].
Анализ изменения КЖ (опросник QOLID-PV) за период 24 недели у пациентов с СД и гипертензией на фоне фармакотерапии обнаружил улучшение показателей КЖ на 30,56% (95% ДИ: 14,30–10,90) для группы амлодипина на 30,94% (95% ДИ: 14,21–10,68) для группы рамиприла на 28,07% (95% ДИ: 14,89–11,20) для группы телмисартана и на 28,84% (95% ДИ: 15,49–11,77) для группы комбинации рамиприла с телмисартаном [43].
Положительное влияние иРААС на КЖ при СД и ХБП было подтверждено в исследовании, включившем использование модели Маркова для анализа затраты – эффективность и определение показателя QALY. Согласно модели Маркова, использование иРААС улучшало показатель QALY с 2,41 до 3,16 года для пациентов с СД и ХБП и с 2,37 до 3,20 для пациентов с ХБП без СД. Дополнительные коэффициенты рентабельности для этих групп составили 2353,39 и 2005,22 долл. США соответственно [44].
Влияние иНГЛТ2 на КЖ пациентов с СД2 представлено во многих исследованиях. В работе S. Grandy и соавт. (2014) исследовалось влияние дапаглифлозина на КЖ пациентов с СД2, получавших метформин (24-недельное двойное слепое рандомизированное плацебо-контролируемое исследование с 78-недельным дополнительным периодом для оценки эффекта дапаглифлозина в комбинации с метформином). Параметры КЖ (EQ-5D) оценивали исходно, через 24, 50 и 102 недели. Исходное значение индекса EQ-5D составило 0,85+0,16 для группы дапаглифлозина и 0,82+0,15 для плацебо. На 102-й неделе значения составили 0,85+0,19 и 0,84+0,19 соответственно, что свидетельствовало об отсутствии выраженного влияния дапаглифозина на КЖ пациентов [45]. Противоположные результаты в отношении влияния на КЖ были получены в японском исследовании, где дапаглифлозин обнаружил не только способность значимо улучшать КЖ пациентов с СД2, но и превосходство по данному параметру по сравнению с ингибиторами дипептидилпептидазы-4 (иДПП-4): показатели КЖ на 24-й неделе были на 28,4% выше в группе дапаглифлозина по сравнению с иДПП-4 [46]. Отмечалось положительное влияние применения дапаглифлозина на уровень КЖ пациентов с сердечно-сосудистыми патологиями. В ретроспективном анализе исследования DELIVER дапаглифлозин по сравнению с плацебо продемонстрировал значительные улучшения в широком диапазоне отдельных компонентов опросника KCCQ (Kansas City Cardiomyopathy Questionnaire) через 8 месяцев у пациентов с сердечной недостаточностью и умеренно сниженной или сохраненной фракцией выброса. Максимальное улучшение наблюдалось в областях частоты симптомов («клиническая оценка») и «физических ограничениях». Сходные результаты были отмечены и в лонгитюдном анализе, который объединял данные за 1, 4 и 8 месяцев [47].
Финеренон доказал значительную клиническую эффективность у пациентов с ХБП на фоне СД2, снижая уровень смертности, темпы прогрессирования ХБП, предотвращая развитие тяжелой почечной недостаточности и потребности в гемодиализе [48–55]. Оценка влияния финеренона на исходы у пациентов с СД2 и ХБП представлена в исследованиях FIDELIO-DKD и FIGARO-DKD, а также в объединенном анализе данных исследований – FIDELITY. По данным FIDELIO-DKD, на основании абсолютной межгрупповой разницы в 3,4% (95% ДИ 0,6–6,2) через 3 года число пациентов, которым необходимо лечение финереноном для предотвращения одного первичного исхода (почечная недостаточность, снижение СКФ на 40% от исходного значения, смерть вследствие ХБП), составило 29 (95% ДИ: 16–166). В отношении вторичных исходов (смерть от сердечно-сосудистых причин, нефатальный инфаркт миокарда, нефатальный инсульт или госпитализация по поводу сердечной недостаточности) это число (NNT) составило 42 (95% ДИ: 22–397) [56]. В исследовании FIDELIO-DKD оценивалось КЖ с использованием двух инструментов: KDQOL-36 и EuroQoL (EQ-5D-5L) – результаты пока не опубликованы. По данным исследования FIGARO-DKD, число пациентов, нуждавшихся в лечении финереноном для предотвращения одного первичного исхода (частота летальных исходов вследствие сердечно-сосудистых причин, нефатального инфаркта миокарда, нефатального инсульта или госпитализации по поводу сердечной недостаточности), составило 47 (95% ДИ: 26–226) на основании абсолютной разницы между группами в 2,1 процентного пункта (95% ДИ: 0,4–3,8) через 3,5 года [57]. Согласно результатам FIDELITY, основываясь на разнице риска между группами в 2,2% через 3 года, число пациентов, нуждавшихся в лечении финереноном для предотвращения одного композитного сердечно-сосудистого исхода (время до смерти от сердечно-сосудистых заболеваний, нефатальный ИМ, нефатальный инсульт или госпитализация по поводу сердечной недостаточности), составило 46 (95% ДИ: 29–109) [58].
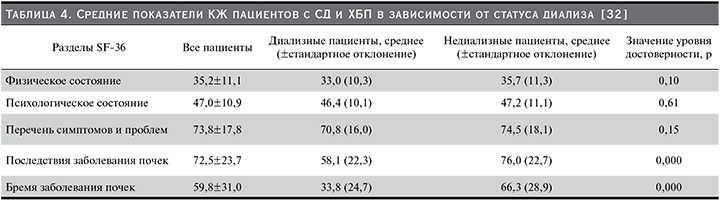
Данные о сравнительном влиянии финеренона и эплеренона на КЖ (опросник KCCQ) пациентов с СД и ХБП были получены в исследовании G. Filippatos и соавт. (2016) [59]. Результаты представлены в табл. 3.
Оценивая комплексное влияние препаратов, способствующих торможению прогрессирования ХПБ и предотвращающих развитие терминальной стадии ХБП, можно отметить их однозначное влияние на параметры КЖ пациентов с СД. Предотвращение необходимости в гемодиализе у пациентов с СД2 является одним из наиболее значимых факторов, способствующих повышению КЖ, о чем свидетельствуют данные работы E. Zimbudzi и соавт. (2016) [32]. Табл. 4 иллюстрирует параметры КЖ пациентов с СД в зависимости от диализного статуса, указывая на минимальное КЖ для пациентов, находящихся на гемодиализе.
Заключение
Оценка КЖ у пациентов с СД может быть осуществлена при помощи как универсальных, так и диабет-специфических опросников.
Развитие ХБП является одним из наиболее значимых факторов риска снижения КЖ пациентов с СД. Значительное снижение КЖ характерно для пациентов с 3б–5-стадиями ХБП, минимальные значения отмечаются при гемодиализе [35]. Пациенты с 5-й стадией ХБП, находящиеся на гемодиализе, испытывают тягостные симптомы, которые крайне негативно влияют на их КЖ, существенно ограничивая возможности для ведения активной жизни. Одним из важных параметров эффективности фармакотерапии СД и ХБП является улучшение показателей КЖ [35]. Одними из первых препаратов, обнаруживших значимое положительное влияние на состояние почек при СД, были иАПФ и БРА, ввиду их способности снижать скорость прогрессирования ХБП, что лежит в основе демонстрируемого ими улучшения показателей КЖ [40–44].
Опубликованные данные не включают информации о положительном влиянии иНГЛТ-2 на КЖ пациентов с ХБП. Повышение КЖ, продемонстрированное в исследованиях, посвященных иНГЛТ2, отмечалось прежде всего в популяции пациентов с СД2 и хронической сердечной недостаточностью [38–42].
Финеренон является препаратом, оказывающим выраженное положительное влияние на течение ХБП у пациентов с СД2, при этом снижая риски развития сердечно-сосудистых осложнений [56–58]. По данным G. Filippatos и соавт. (2016), КЖ пациентов с СД2 и ХБП значительно улучшалось при применении финеренона в дозе от 5 до 20 мг/сут. [59]. Снижение рисков развития сердечно-сосудистых осложнений, улучшение почечной функции, снижение темпов прогрессирования ХБП, предотвращение потребности в гемодиализе, продемонстрированные финереноном в таких исследованиях, как FIDELIO-DKD, FIGARO-DKD и FIDELITY, являются основными факторами улучшения КЖ пациентов с СД2 и ХБП. Таким образом, применение финеренона позволит отдалить развитие терминальной почечной недостаточности и необходимость проведения диализа и трансплантации, обеспечивая кардио- и нефро-протекцию, положительно влияя на КЖ пациентов.



