Введение
За последние 10 лет в диализной популяции отмечен рост числа пациентов пожилого и старческого возраста [1]. Одной из основных особенностей пациентов этой когорты является наличие высокого коморбидного фона, затрагивающего сердечно-сосудистую, нервную, мышечно-скелетную и другие системы, что определяет высокую заболеваемость и смертность у лиц старше 60 лет, начинающих лечение почечно-заместительной терапией (ПЗТ) [2].
По данным обсервационных исследований, у пациентов с тяжелой сопутствующей патологией диализ не обеспечивает значимого продления жизни, но при этом может негативно влиять на функциональный статус, когнитивную функцию, увеличивать число госпитализаций и способствовать прогрессированию ряда осложнений [3–5]. Таким образом, объективная оценка коморбидного фона может помочь выбрать правильную модальность/режим лечения и улучшить качество жизни.
В настоящее время известно более 30 методов измерения мульти- и коморбидности [6], среди них наибольшую валидность и достоверность имеют следующие шкалы [7]: кумулятивная шкала оценки заболеваемости (CIRS) 1968 г., индекс Каплана-Файнштейна (KFI) 1987 г., индекс коморбидности Чарлсон (ИКЧ, CCI) 1987 г., гериатрическая кумулятивная шкала оценки заболеваемости (CIRS-G) 1991 г., чек-лист тяжести заболеваний Дюка (DUSOI Index) 1993 г., индекс сосуществующих болезней (ICED) 1993 г.
Все перечисленные шкалы активно используются в медицинских исследованиях и клинической практике, однако наибольшую распространенность за удобство в использовании получил ИКЧ, предложенный Dr. Mary E. Charlson [8].
В разных областях медицины ИКЧ показал свою эффективность в объективной оценке уровня коморбидности и риска летального исхода [9–13], в т.ч. и у пациентов с терминальной стадией хронической болезни почек (ХБП) [14–16].
Цель: оценить прогностическую роль ИКЧ как предиктора неблагоприятного исхода в когорте пациентов в возрасте 60 лет и старше, начинающих лечение хроническим диализом.
Материал и методы
С января 2017 по январь 2023 г. 563 пациента в возрасте ≥18 лет начали лечение программным диализом в учреждении здравоохранения «1-я городская клиническая больница». Пациентов не включали в настоящее исследование, если они: 1) были моложе 60 лет на момент начала диализа; 2) имели острое почечное повреждение (ОПП); 3) при отсутствии полной информации о пациенте.
Таким образом, когорта исследования (рис. 1) состояла из 246 пациентов (49,2% мужчин и 50,8% женщин) в возрасте от 60 до 83 лет (медиана возраста 68 лет), медиана наблюдения составила 2 года (1,5; 2,5).

Всем пациентам было проведено комплексное клиническое обследование, включавшее измерение суточного диуреза, оценку статуса гипергидратации по данным физикального осмотра и рентгенологических признаков застоя по малому кругу кровообращения и/или гидроторакса. Лабораторные исследования креатинина (мкмоль/л), мочевины (ммоль/л) и калия (ммоль/л) в сыворотке крови проводились по стандартной методике, скорость клубочковой фильтрации (СКФ) рассчитывали по формуле CKD-EPI [17]. Модальность диализа (программный гемодиализ – ПГД) или постоянный амбулаторный перитонеальный диализ (ПАПД)) определялась на момент начала ПЗТ. Уровень коморбидности измерялся с использованием шкалы ИКЧ [8], при этом учитывая, что ХБП в данном исследовании имелась у всех пациентов и рассматривалась в качестве основной патологии, при присуждении баллов по шкале ИКЧ этот показатель исключался и не учитывался.
За клиническую конечную точку был принят летальный исход, а цензурирование проводилось в случаях окончания периода наблюдения (пациент продолжил лечение после 23.07.2023), выполненной трансплантации почки, перевода на лечение в другое учреждение здравоохранения, прекращения диализа.
Анализ соответствия вида распределения количественных показателей закону нормального распределения выполняли с использованием критерия Шапиро–Уилка. Все показатели в данном исследовании имели отклонения от нормального распределения, поэтому количественные показатели исследования представлены медианой и квартилями в виде Me (Q25; Q75). Качественные показатели представлены в виде абсолютных (n) и относительных (%) значений.
Анализ выживаемости осуществляли с помощью оценки Каплана–Майера, определялась кумулятивная вероятность дожития.
Для выявления факторов риска в однофакторном и многофакторном анализах использовалась полупараметрическая модель пропорциональных рисков Кокса. Факторы риска оценивали на основании отношения рисков (ОР) и представлены как ОР (95% доверительный интервал – ДИ). Для установления уровня количественного показателя, ассоциированного с риском неблагоприятного исхода, использовался метод максимальной ранговой статистики [18].
Статистическую обработку данных проводили с использованием статистического пакета R, версия 4.1.3., и библиотек survival, survminer, maxstat.
Для статистических выводов ошибка первого рода была принята α=0,05.
Результаты
Исходные данные пациентов представлены в (табл. 1).
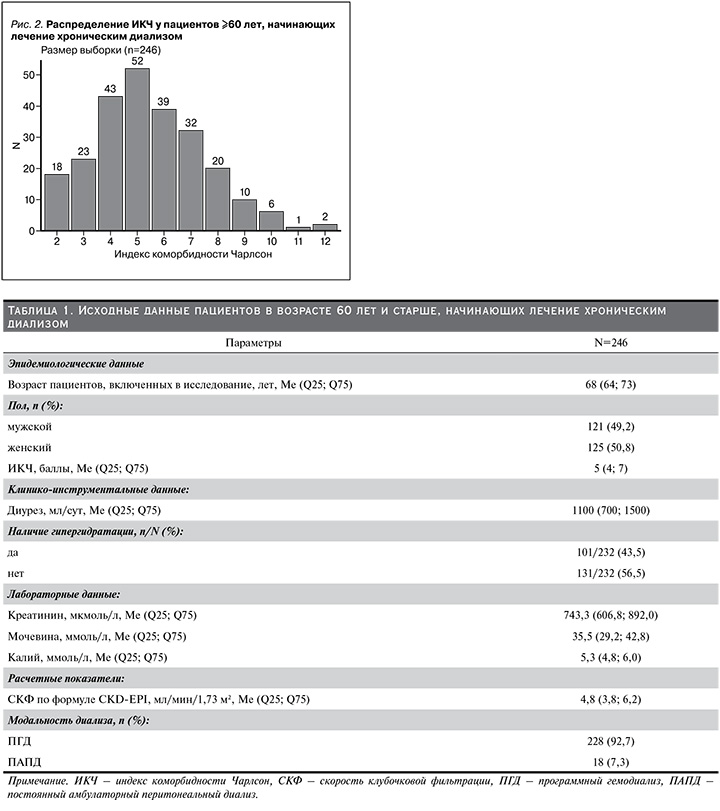
Медиана возраста когорты составила 68 (64; 73) лет, большинство пациентов (92,7%) получали лечение методом ПГД.
Распределение ИКЧ в исследуемой когорте представлено на рис. 2. Бóльшая часть пациентов пожилого и старческого возраста, начинающих лечение хроническим диализом, имели ИКЧ 5 баллов (52/21,1%)), значительная доля пациентов имели ИКЧ 4 (43/17,5%) и 6 баллов (39/15,9%) и ИКЧ варьировался в диапазоне от 2 до 12 баллов.
Период наблюдения за пациентами составил 2 (1,5; 2,5) года. Летальный исход был зарегистрирован у 156 (63,4%) пациентов. Медиана выживаемости составила 386 дней. Кумулятивная выживаемость когорты исследования представлена на рис. 3.
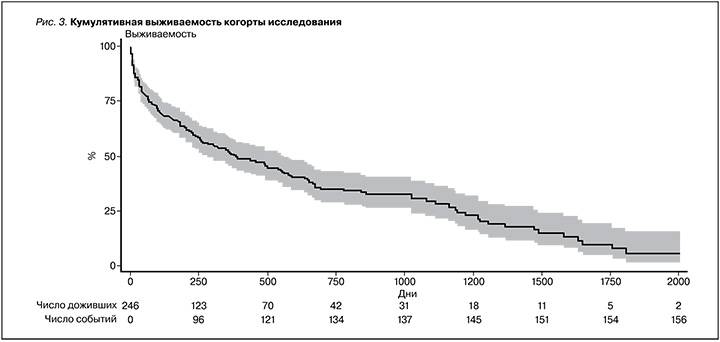
С целью определения предикторов летального исхода (ПЛИ) проведен однофакторный регрессионный анализ (табл. 2).
Все статистически значимые показатели при однофакторном регрессионном анализе включены в многофакторный анализ со своими пороговыми значениями. При многофакторном анализе наличие симптомов гипергидратации и состояние остаточной функции почек утратили свою значимость, а независимыми ПЛИ явились: возраст >65 лет (ОР=1,7, 95% ДИ 1,1–2,4; p=0,009), ИКЧ>5 баллов (ОР=3, 95% ДИ 2–4,4; p<0,001), преддиализный уровень креатинина ≤514 мкмоль/л (ОР=2,7, 95% ДИ 1,7–4,5; р<0,001) и преддиализный уровень мочевины в сыворотке крови >44 ммоль/л (ОР=1,8, 95% ДИ 1,2–2,9; р=0,009) (табл. 3).
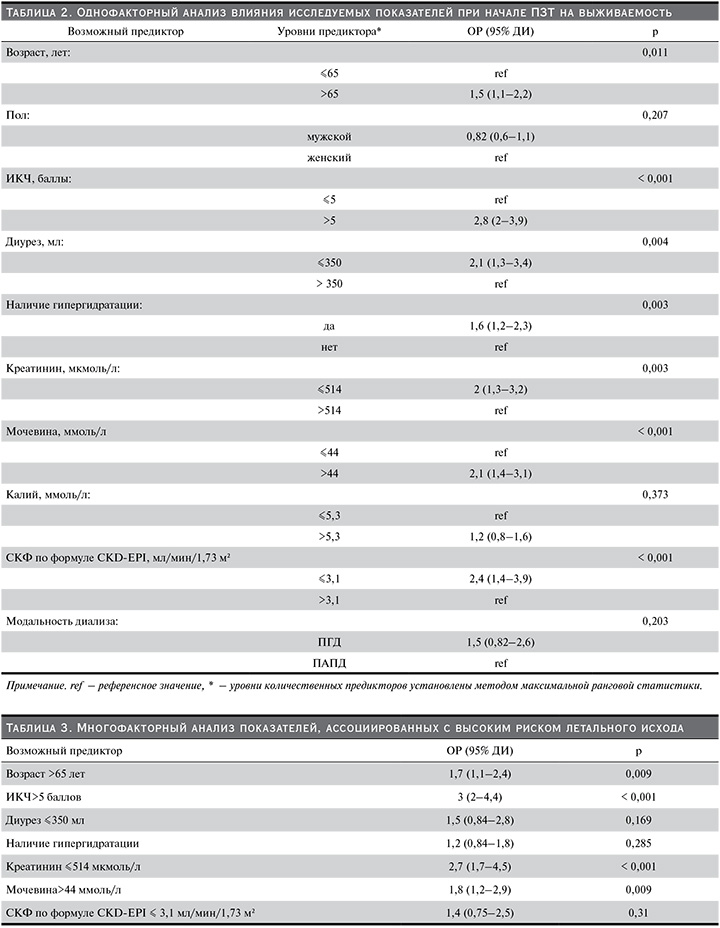
Таким образом, по результатам многофакторного анализа выявлено, что факторами риска неблагоприятного исхода у пациентов ≥60 лет, начинающих лечение программным диализом, являются преддиализный уровень креатинина ≤514 мкмоль/л, мочевины >44 ммоль/л, возраст >65 лет и ИКЧ>5 баллов.
Обсуждение
По данным Европейского регистра ПЗТ (ERA Registry) за 2019 г., средний возраст начала диализа составил 65 лет, при этом доля пациентов от 65 до 74 лет достигла 28%, а доля пациентов ≥75 лет – 26%, что свидетельствует о том, что более половины пациентов, начинающих ПЗТ, являются лицами пожилого и старческого возраста [1].
В то же время отмечается низкая выживаемость в этой группе пациентов. Так, среди 391 пациента в возрасте 65 лет и старше из североамериканской базы Medicare, 88 (23%) человек умерли в течение первого месяца лечения, 173 (45%) – в течение 6 месяцев и 213 (55%) – в течение года лечения диализом, что почти вдвое превышает годовой уровень смертности, зарегистрированный у пожилых пациентов в США [19].
Все это обусловливает поиск новых инструментов для оценки прогноза в диализной популяции. Одним из удобных и валидных методов оценки является ИКЧ, который, как было показано, ассоциирован с риском 30-дневной повторной госпитализации диализных пациентов, кроме того, он может быть использован для стратификации риска повторной госпитализации в данной когорте пациентов [20].
По результатам нескольких исследований ИКЧ являлся независимым фактором неблагоприятного прогноза для вновь взятых на лечение ПГД пациентов в возрасте ≥18 лет [15, 16], при этом в части исследований данной тенденции отмечено не было [21]. Так, в исследовании Yee-Yung Ng и соавт., включавшем 7391 пациента, начинающего лечение ПГД, показано, что наличие высокого ИКЧ на додиализном этапе влияет на выживаемость пациентов на ПЗТ [15]. В другой работе у компенсированных гемодиализных пациентов наличие высокого модифицированного ИКЧ (ИКЧ без учета возраста) достоверно повышало риск летального исхода [16]. Однако наблюдение E. McArthur и соавт. не выявило статистически достоверной связи между ни одним из 5 индексов (ИКЧ, модифицированный ИКЧ, шкала загрегированных диагностических групп Джона Хопкинса, индекс Эликсхаузера и индекс Райта–Хана) и годовой летальностью пациентов с ХБП [21].
В проведенном нами исследовании выявлена высокая распространенность ИКЧ>5 баллов в пожилой диализной популяции, доля пациентов с величиной ИКЧ 6–12 баллов составила 44,7%. Проведенный многофакторный анализ показал, что ИКЧ>5 баллов у пациентов в возрасте ≥60 лет с ХБП С5 является дополнительным независимым ПЛИ и увеличивает риск неблагоприятного исхода в 3 раза (95% ДИ 2–4,4; р<0,001), что требует от врача-нефролога оптимизации оказания медицинской помощи пациентам пожилого и старческого возраста уже на преддиализном этапе.
Таким образом, пациентам в возрасте >65 лет с ИКЧ>5 баллов при достижении ими диализного уровня уремии следует проводить не только стандартные методы диализотерапии, но и рассматривать альтернативные виды ПЗТ, а именно поддерживающие режимы диализа [22], а также паллиативное консервативное лечение [23, 24].
В проведенном ранее нами исследовании показана эффективность ПАПД над ПГД у пациентов пожилого и старческого возраста, где выживаемость на первом году составила 81,2±9,8% на ПАПД против 46,5±3,8% на ПГД, при этом не было выявлено значимых различий в 2-летней выживаемости – 33,3±3,9% на ПГД против 37,2±13% на ПАПД [25]. Таким образом, данный вариант ПЗТ может рассматриваться как лучшая альтернатива ПГД лицам пожилого возраста с наличием высокой коморбидности, принимая во внимание, что это домашний вид диализа, особенно при наличии обученного ассистента (волонтер, родственник и/или патронажная медицинская сестра).
Поддерживающие режимы ПЗТ направлены на купирование острой уремической симптоматики и не требуют достижения целевых показателей лечения (целевого уровня Кt/V, гемоглобина, показателей кальциево-фосфорного обмена и т.д.). Они представляют собой 2 обмена в сутки для ПАПД и сеансы по 2 часа 2–3 раза в неделю для ПГД.
С другой стороны, не все пациенты в состоянии перенести лечение ПГД или ПАПД, нарастающее число осложнений, связанных с сердечно-сосудистой, дыхательной системами, прогрессирующее снижение когнитивной функции требует принятие решения о проведении консервативного лечения. Важно отметить, что консервативная паллиативная терапия не направлена на лечение самой ХБП, а скорее на улучшение общего состояния пациента, снижение симптомов и поддержку его комфорта и качества жизни. Результаты проведенного исследования среди лиц старше 70 лет продемонстрировали, что для пациентов в возрасте старше 80 лет с низким функциональным статусом или высоким ИКЧ (≥8 баллов), ПЗТ не имела никаких преимуществ в плане выживаемости, при этом пациенты в группе консервативного лечения имели меньшую вероятность госпитализации и более высокое качество жизни [4].
Основным ограничением данного исследования является его характер: данное исследование представляет собой историческое когортное исследование, когорта была выделена по картам пациентов и прослежена до настоящего момента времени. Кроме того, в группах пациентов с разным функциональным статусом не проверялись различия значений ИКЧ и не проводилось сравнения эффективности шкалы ИКЧ и шкал, оценивающих функциональный статус у пациентов пожилого и старческого возраста с ХБП С5. Все это требует дальнейшего изучения на больших когортах пациентов пожилого и старческого возраста с ХБП С5.
Заключение
В настоящее время показания к началу лечения и выбору метода ПЗТ основываются на показателях уремии, кислотно-основного состояния крови, статуса гидратации, тогда как все большее число научных работ свидетельствует о необходимости определения индексов коморбидности как интегральных и объективных маркеров неблагоприятного прогноза. В нашей работе ИКЧ зарекомендовал себя как простой и легко воспроизводимый способ оценки риска летального исхода у пациентов пожилого и старческого возраста с ХБП С5. Включение его в клинический протокол диализного лечения пациентов с ХБП позволит продолжить совершенствование персонализированного подхода в системе здравоохранения, который предполагает совместное принятие решений между врачом и пациентом в выборе соответствующего варианта ПЗТ.



